1. (Unaerp-SP) O fenômeno da supercondução de eletricidade, descoberto em 1911, voltou
a ser objeto da atenção do mundo científico com a constatação de Bednorz e
Muller de que materiais cerâmicos podem exibir esse tipo de comportamento,
valendo um prêmio Nobel a esses físicos em 1987. Um dos elementos químicos mais
importantes na formulação da cerâmica supercondutora é o ÍTRIO:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d1.
O número de camadas e o número de elétrons
mais energéticos para o ítrio serão, respectivamente:
a) 4 e 1.
b) 5 e 1.
c) 4 e 2.
d) 5 e 3.
e) 4 e 3.
2. (Ufrs) O íon
monoatômico A2- apresenta a configuração eletrônica 3s2 3p6 para o último
nível. O número atômico do elemento A é:
a) 8
b) 10
c) 14
d) 16
e) 18
3. (Cesgranrio) A distribuição eletrônica do átomo 26Fe, em camadas, é:
a) 1s2 2s2 2p6
3s2 3p6 4s2 3d6.
b) 1s2 2s2 2p6
3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2.
c) K = 2; L = 8;
M = 16.
d) K = 2; L = 8; M = 14; N = 2.
e) K = 2; L = 8;
M = 18; N = 18; O = 8; P = 2.
4. (Unifor-CE) O átomo de um elemento químico tem 14 elétrons no terceiro nível
energético (n = 3). O número atômico desse elemento é:
a) 14
b) 16
c) 24
d) 26
e) 36
5. (IFSP/2013) O número de elétrons da camada de valência do átomo de cálcio (Z = 20),
no estado fundamental, é:
a) 1.
b) 2.
c) 6.
d) 8.
e) 10.
6. (FM Petrópolis RJ/2013) O chumbo é um metal pesado que pode contaminar o ar, o solo, os rios e
alimentos. A absorção de quantidades pequenas de chumbo por longos períodos
pode levar a uma toxicidade crônica, que se manifesta de várias formas,
especialmente afetando o sistema nervoso, sendo as crianças as principais
vítimas. Sendo o número atômico (Z) do chumbo igual a 82, o íon plumboso (Pb+2)
possui os elétrons mais energéticos no subnível:
a) 6p2
b) 6s2
c) 6p4
d) 5d10
e) 4f14
7. (PUC) O
número normal de subníveis existentes no quarto nível energético dos átomos é
igual a:
a) 2
b) 5
c) 3
d) 1
e) 4
8. (OSEC) Sendo
o subnível 4s1 (com um elétron) o mais energético de um átomo, podemos afirmar
que:
I. o número
total de elétrons desse átomo é igual a 19;
II. esse
apresenta quatro camadas eletrônicas;
III. a sua
configuração eletrônica é 1s2 2s2 2p6 3s2 3p6 3d10 4s1
a) Apenas a
firmação I é correta.
b) Apenas a
firmação II é correta.
c) Apenas a
firmação III é correta.
d) As afirmações
II e III são corretas.
e) As afirmações I e II são corretas.
9. (UFSC) O
número de elétrons em cada subnível do átomo estrôncio (38Sr) em ordem
crescente de energia é:
a) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2
b) 1s2 2s2 2p6
3s2 3p6 4s2 4p6 3d10 5s2
c) 1s2 2s2 2p6
3s2 3p6 3d10 4s2 4p6 5s2
d) 1s2 2s2 2p6
3s2 3p6 4p6 4s2 3d10 5s2
e) 1s2 2s2 2p6
3p6 3s2 4s2 4p6 3d10 5s2
10. (Unificado-RJ) - As torcidas vêm colorindo cada vez mais os estádios de futebol com
fogos de artifício. Sabemos que as cores desses fogos se devem à presença de
certos elementos químicos. Um dos mais usados para obter a cor vermelha é o
estrôncio (Z = 38), que, na forma do íon Sr+2, tem a seguinte configuração
eletrônica:
a) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6
b) 1s2 2s2 2p6
3s2 3p6 4s2 3d10 4p6 5s2
c) 1s2 2s2 2p6
3s2 3p6 4s2 3d10 4p6 5s2 5p2
d) 1s2 2s2 2p6
3s2 3p6 4s2 3d10 4p6 4d2
e) 1s2 2s2 2p6
3s2 3p6 4s2 3d10 4p4 5s2
11. (Mack-2003) Uma distribuição eletrônica possível para um elemento X, que pertence à
mesma família do elemento bromo, cujo número atômico é igual a 35, é:
a) 1s2, 2s2,
2p5
b) 1s2, 2s2,
2p6, 3s2, 3p1
c) 1s2, 2s2, 2p2
d) 1s2, 2s2,
2p6, 3s1
e) 1s2, 2s2,
2p6, 3s2, 3p6, 4s2, 3d5
12. (UNI-RIO) “Os implantes dentários estão mais seguros no Brasil e já atendem às
normas internacionais de qualidade. O grande salto de qualidade aconteceu no
processo de confecção dos parafusos e pinos de titânio, que compõem as
próteses. Feitas com ligas de titânio, essas próteses são usadas para fixar
coroas dentárias, aparelhos ortodônticos e dentaduras, nos ossos da mandíbula e
do maxilar.”
Jornal do Brasil, outubro 1996.
Considerando que o número atômico do titânio
é 22, sua configuração eletrônica será:
a) 1s2 2s2 2p6
3s2 3p3
b) 1s2 2s2 2p6
3s2 3p5
c) 1s2 2s2 2p6
3s2 3p6 4s2
d) 1s2 2s2 2p6 3s2 3p6 4s2 3d2
e) 1s2 2s2 2p6
3s2 3p6 4s2 3d10 4p6
13. (AMAN-SP) O elemento hipotético com nº atômico (Z = 116) apresenta na camada mais
externa (camada de valência) um número de elétrons igual a:
a) 2
b) 4
c) 6
d) 8
e) 18
14. (ITA-SP) No esquema a seguir, encontramos duas distribuições eletrônicas de um
mesmo átomo neutro:
A 1s2 2s2
B 1s2 2s1
2p1
A seu respeito é correto afirmar:
a) A é a
configuração ativada.
b) B é a
configuração normal (fundamental).
c) A passagem de
A para B libera energia na forma de ondas eletromagnéticas.
d) A passagem
de A para B absorve energia.
e) A passagem de
A para B envolve perda de um elétron.
15. (FEI-SP) A configuração eletrônica de um átomo neutro no estado fundamental é
1s2 2s2 2p6 3s2 3p5. O número de orbitais vazios remanescentes no nível
principal M é:
a) 0
b) 1
c) 5
d) 6
e) 10
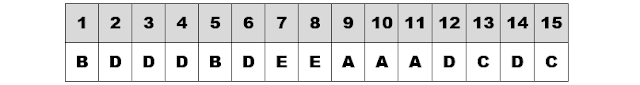
GABARITO
























0 Comentários